
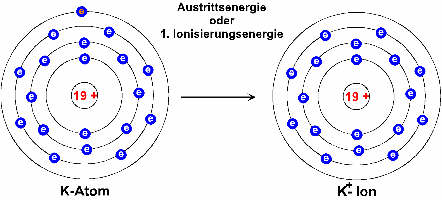
Wird dem Kaliumatom mehr Energie als die Austrittsenergie zugeführt, so wird der überschüssige Energiebetrag in Kinetische Energie umgewandelt, die auf das Atom und das Elektron übertragen wird. Da die Masse des Atoms um den Faktor 1000 größer ist, als die Elektronenmasse, nimmt das Elektron über 99,9999% der kinetischen Energie mit.
Befindet sich das Elektron nun selbst in einem Elektrischen Feld, so kann es beschleunigt oder abgebremst werden. Wählt man über die Spannung die Stärke des Elektrischen Feldes gerade so, dass das Elektron seine gesamte kinetische Energie verliert, so gelangen keine Elektronen von der Kaliumschicht zur Gegenelektrode, der Stromfluss ist dann gleich Null. Die dazu benötigte Elektrische Energie ist also genauso groß wie die kinetische Energie des Elektrons. Daraus ergibt sich eine einfache Beziehung:
| Eelektrisch = Ekinetisch
ELicht = EAustritt + Ekinetisch ELicht = EAustritt + Eelektrisch |
Die Austrittsenergie ist eine Stoffkonstante, die Kinetische Energie wird über die Messung der Elektrischen Energie ( E = e*U) bestimmt. Damit kann dann die Energie des Photons (ELicht) berechnet werden.
Ist die Austrittsarbeit unbekannt, so wird die Messung bei mehreren
Frequenzen
des Lichtes durchgeführt und die Frequenz des Lichtes gegen die
Gegenspannung aufgetragen. Die dabei ermittelte Grenzfrequenz
(Schnittpunkt
mit der Y-Achse) ist proportional zur Austrittsarbeit.
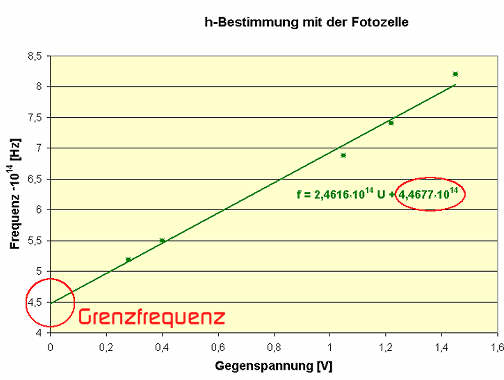
Misst man bei mehreren Frequenzen, so zeigt sich, dass ein linearer Zusammenhang zwischen der Frequenz und der Energie des Lichtes besteht. Dieser Proportionalitätsfaktor wird nach seinem Entdecker das Planck`sche Wirkungsqantum (h) bezeichnet. Es hat den Wert